Uniklinikum Würzburg: Studie mit bispezifischem Antikörper liefert beeindruckende Behandlungserfolge bei Multiplem Myelom
Eine mehrjährige Phase I-Studie zeigte, dass die Therapie mit dem bispezifischen Antikörper AMG 420 bei Patienten mit fortgeschrittenem Multiplem Myelom hervorragende Ergebnisse erzielen kann. Das Uniklinikum Würzburg konzipierte das multizentrische Projekt und schloss auch die meisten Patienten ein.
Ein Artikel in der März-Ausgabe der US-amerikanischen medizinischen Fachzeitschrift Journal of Clinical Oncology fasst die großen Erfolge zusammen, die eine Phase I-Studie mit dem bispezifischen Antikörper AMG 420 bei der Behandlung von Patienten mit Multiplem Myelom erzielen konnte. Die bösartige Krebserkrankung des blutbildenden Systems gilt derzeit als noch nicht heilbar. Nach der in der Studie erprobten Immuntherapie konnte allerdings bei 50 Prozent der Patienten der Tumor selbst mit den empfindlichsten Diagnosemethoden nicht mehr nachgewiesen werden.
An dem vor rund drei Jahren gestarteten und Mitte 2019 beendeten Vorhaben waren neben drei französischen Krebsforschungszentren auch die Universitätsklinika in Ulm und Würzburg beteiligt. Eine führende Rolle spielte die Medizinische Klinik und Poliklinik II des Uniklinikums Würzburg (UKW): Die von Prof. Dr. Hermann Einsele geleitete Klinik konzipierte die Studie und rekrutierte auch die meisten Teilnehmer/innen. „Für die ansonsten austherapierten Patienten mit fortgeschrittener Erkrankung war die Studienteilnahme eine erneute Chance auf eine Verbesserung ihrer Situation“, berichtet Prof. Einsele.
Ein Antikörper mit zwei Zielproteinen
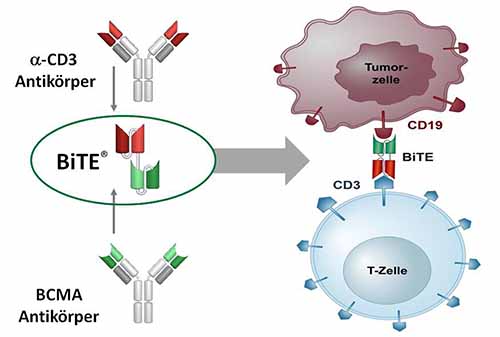
Wie funktioniert der eingesetzte Wirkstoff? „AMG 420 ist ein gentechnisch designter Antikörper, der mit der BiTE-Technologie des Biotec-Unternehmens Amgen hergestellt wird. Er hat zwei Zielproteine, weshalb man ihn auch als ‚bispezifisch‘ bezeichnet“, erläutert Prof. Dr. Max Topp, der Studienleiter der AMG 420-Studie. Der Schwerpunktleiter Hämatologie an der Medizinischen Klinik II des UKW und Erstautor der Studienpublikation fährt fort: „Das erste Ziel ist das B-Zell-Reifungsantigen BMCA, das hauptsächlich auf Myelomzellen vorkommt. Das zweite ist CD3, ein Protein das auf der Oberfläche von T-Zellen – den effektivsten körpereigenen Abwehrzellen – zu finden ist.“ Mit der Kopplung an diese beiden Proteine zieht AMG 420 T-Zellen an die Krebszellen und bindet sie dort. So werden die Killerzellen in die Lage versetzt, die Myelomzellen, die sich ansonsten durch eine biochemische Tarnung vor dem Zugriff der T-Zellen schützen, zu vernichten.
Dauerinfusion in mehreren Zyklen
Wie lief die Phase I-Studie ab? Insgesamt erhielten 42 Patienten per Infusion den Wirkstoff. Hierbei ging es zunächst darum, unter Abwägung der Wirksamkeit und der Nebenwirkungen die richtige Dosierung zu finden. „Als Nebenwirkung kann es bei dieser Therapie zu einer Überreaktion des Immunsystems, dem sogenannten Zykotin-Freisetzungssyndrom, kommen sowie bei einer Minderheit der Patienten auch zu schwerwiegenden infektiöse Komplikationen“, schildert Prof. Topp. Bei der Studie wurde ermittelt, dass 400 Mikrogramm pro Tag die beste Dosis ist. Diese Medikamentenmenge wurde anschließend zehn Patienten verabreicht – jeweils in mehreren Zyklen und per Dauerinfusion. Pro Zyklus wurde dabei die Infusionslösung vier Wochen lang mit einer Pumpe über einen festen Venenzugang zugeführt, gefolgt von einer zweiwöchigen Therapiepause. Je nach der individuell unterschiedlichen Anzahl an Zyklen dauerte die Behandlung bis zu 60 Wochen.
Hochwirksam – bis zur Totalremission
Was war das Ergebnis? Sieben der zehn Patienten erreichten zumindest eine signifikante Remission, bei fünf Patienten konnte sogar keine minimale Resterkrankung mehr erkannt werden. Das heißt: Es waren selbst mit den feinsten Messmethoden keine Myelomzellen mehr nachweisbar. Diese Totalremission hält bei manchen Studienteilnehmern schon seit mittlerweile rund einem Jahr an, die Krebserkrankung ist bei ihnen bislang nicht zurückgekehrt. „Auch die Nebenwirkungen hielten sich insgesamt in einem sehr akzeptablen Rahmen. So war bei keinem unserer Studienpatienten eine Intensivbehandlung notwendig“, freut sich Prof. Einsele.
Vielleicht schon in zwei Jahren Teil der Routineversorgung
„Wir haben diese Ergebnisse in den vergangenen Monaten schon auf mehreren internationalen Krebskongressen vorgestellt, wo sich die Myelom-Expertenszene durchweg sehr beeindruckt zeigte“, berichtet Prof. Topp. Und Prof. Einsele ergänzt: „Ich denke, man kann hier mit Fug und Recht von einem Meilenstein in der Myelom-Therapie sprechen.“ Laut dem Klinikdirektor und Letztautor der Studie wurde das Prinzip der bispezifischen Antikörpertherapie zwischenzeitlich von vielen Firmen aufgenommen. Neue Studien – weltweit, wie auch in Würzburg – treiben derzeit die Weiterentwicklung voran. Aktuell arbeitet man zum Beispiel daran, die Antikörper so abzuändern, dass statt einer Dauerinfusion eine einmalige Infusion pro Zykluswoche ausreicht. „Möglicherweise kann die Behandlung mit bispezifischen Antikörper schon in ein bis zwei Jahren in die Routineversorgung von Myelom-Patienten übergehen“, hofft Prof. Einsele. Über die letztendlichen Kosten einer entsprechenden Therapie können nach seinen Worten in dieser frühen Entwicklungsphase noch keine Aussagen getroffen werden.
Der mit der BiTE-Technologie hergestellte bispezifische Antikörper ist in der Lage, T-Zellen an die Myelom-Zellen zu binden und so deren Zerstörung einzuleiten.
Bild: Medizinische Klinik II / Uniklinikum Würzburg
Literatur:
Anti–B-Cell Maturation Antigen BiTE Molecule AMG 420 Induces Responses in Multiple Myeloma; Max S. Topp, Johannes Duell, Gerhard Zugmaier, Michel Attal, Philippe Moreau, Christian Langer, Jan Krönke, Thierry Facon, Alexey V. Salnikov, Robin Lesley, Karl Beutner, James Kalabus, Erik Rasmussen, Kathrin Riemann, Alex C. Minella, Gerd Munzert, Hermann Einsele; Journal of Clinical Oncology, Vol. 38, S. 775–783, 2020
